La enfermedad de los cálculos biliares constituye una alteración multifactorial del sistema hepatobiliar caracterizada por la formación de concreciones sólidas dentro de la vesícula biliar como consecuencia de un profundo desequilibrio fisicoquímico y metabólico en la composición de la bilis. Su elevada prevalencia global, estimada entre 10–20%, refleja no solo su amplia distribución geográfica sino también su estrecha relación con los cambios contemporáneos en los estilos de vida, particularmente el incremento sostenido del exceso de peso corporal y de la obesidad visceral.
La asociación entre obesidad y litiasis biliar se sustenta en mecanismos bioquímicos y endocrinos complejos. El hígado desempeña un papel central al regular la síntesis y secreción de colesterol hacia la bilis. En individuos con obesidad, existe una sobreexpresión de transportadores hepáticos responsables de la secreción de colesterol, lo que conduce a una sobresaturación de la bilis con este lípido. Este fenómeno incrementa la probabilidad de nucleación de cristales de colesterol, primer paso en la formación de cálculos. Se ha demostrado que la hipersecreción biliar de colesterol está directamente relacionada con el aumento de la masa grasa corporal y con la resistencia a la insulina, la cual modula negativamente la homeostasis lipídica hepática.
Además de la sobresaturación, la formación de cálculos requiere alteraciones en la cinética de la vesícula biliar. En condiciones normales, la vesícula se contrae de manera eficiente en respuesta a la ingesta de alimentos, mediada principalmente por la acción de la colecistoquinina. Sin embargo, en individuos con obesidad o síndrome metabólico, se observa una disminución en la motilidad vesicular, lo que favorece la estasis biliar. Esta estasis prolonga el tiempo de permanencia de la bilis sobresaturada en la vesícula, facilitando la agregación de cristales y su crecimiento progresivo. Se ha documentado que la disfunción de la contracción vesicular está asociada con alteraciones en la señalización hormonal intestinal y con cambios en la sensibilidad de los receptores de colecistoquinina.
Otro componente fundamental en la fisiopatología es la alteración en la composición de los ácidos biliares. Estos compuestos son esenciales para mantener el colesterol en solución dentro de la bilis. En estados de obesidad, se ha observado una reducción relativa en la concentración de ácidos biliares hidrofílicos, junto con cambios en la microbiota intestinal que afectan su metabolismo. Esta modificación en el pool de ácidos biliares contribuye a la pérdida de estabilidad micelar, favoreciendo la precipitación del colesterol.
El sistema hígado-vesícula biliar-intestino opera como un eje integrado en el cual intervienen múltiples vías de señalización molecular. Entre estas destacan los receptores nucleares que regulan el metabolismo lipídico, como el receptor X de hígado y el receptor farnesoide X, los cuales modulan la síntesis de colesterol y ácidos biliares. Alteraciones en estas vías, inducidas por estados metabólicos como la obesidad y la resistencia a la insulina, contribuyen significativamente al desarrollo de litiasis. Asimismo, enzimas clave en la esterificación del colesterol, como la acil-CoA colesterol aciltransferasa, presentan cambios en su actividad que afectan la disponibilidad de colesterol libre en la bilis.
A pesar de la fuerte asociación con obesidad, la enfermedad también se presenta en individuos con peso corporal normal, lo que evidencia la participación de factores adicionales. Entre los factores no modificables destacan la edad, debido a cambios progresivos en la función hepática y vesicular; el sexo femenino, relacionado con la influencia de los estrógenos en el metabolismo del colesterol; la genética, que condiciona variaciones en transportadores y enzimas; y la etnia, con diferencias observadas en la prevalencia entre poblaciones. La paridad también incrementa el riesgo, probablemente por efectos hormonales acumulativos sobre la motilidad vesicular y la composición biliar.
Por otro lado, los factores modificables incluyen la dieta, particularmente el consumo elevado de grasas saturadas y carbohidratos refinados, que incrementan la síntesis hepática de colesterol; la inactividad física, que contribuye a la resistencia a la insulina; y el uso de ciertos medicamentos, como anticonceptivos orales o terapias hormonales, que alteran el metabolismo lipídico. La pérdida rápida de peso, paradójicamente, también puede inducir litiasis debido a una movilización acelerada de colesterol desde los tejidos adiposos hacia el hígado.
La carga clínica de la enfermedad es considerable, no solo por la necesidad frecuente de intervención quirúrgica mediante colecistectomía, sino también por su asociación con otras patologías metabólicas. Se ha evidenciado una correlación significativa entre litiasis biliar y enfermedades cardiovasculares, atribuida a mecanismos compartidos como la dislipidemia y la inflamación crónica de bajo grado. Asimismo, la presencia de cálculos biliares se ha vinculado con un mayor riesgo de cáncer de vesícula biliar, especialmente en contextos de inflamación crónica y daño epitelial prolongado.
En términos de salud pública, aunque la mortalidad directa es relativamente baja, la morbilidad asociada y los costos del tratamiento justifican la implementación de estrategias preventivas. Estas deben centrarse en la modificación de factores de riesgo, incluyendo el control del peso corporal, la promoción de la actividad física regular y la adopción de patrones dietéticos saludables. La comprensión detallada de los mecanismos moleculares y fisiológicos involucrados en la formación de cálculos biliares permite identificar posibles blancos terapéuticos y desarrollar intervenciones más eficaces.
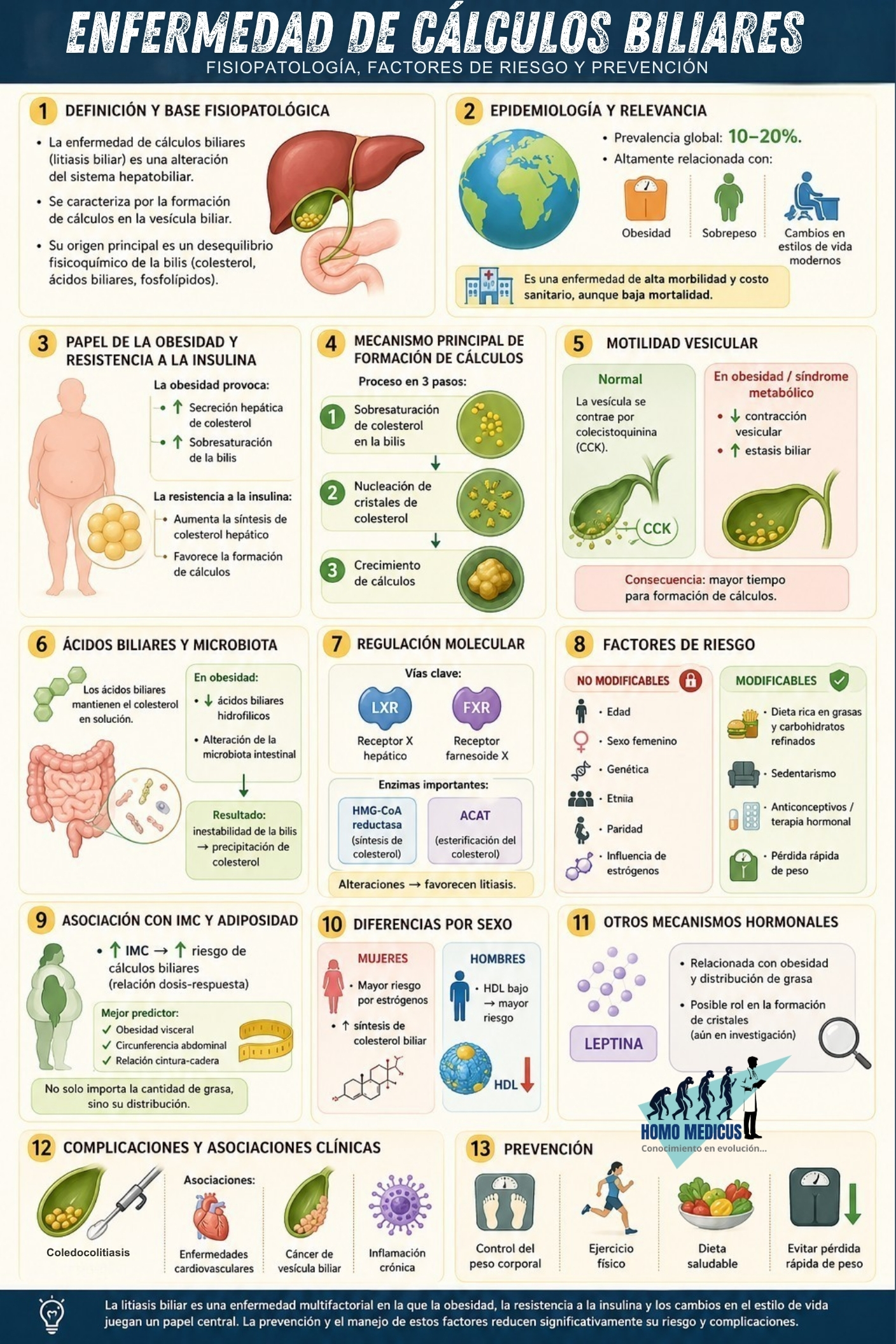
Asociaciones comprobadas con los cálculos biliares
El índice de masa corporal, entendido como la relación entre el peso corporal y el cuadrado de la talla, constituye una aproximación epidemiológica ampliamente validada para estimar el grado de adiposidad total en poblaciones humanas, aunque no discrimina de manera directa la composición corporal entre masa grasa y masa magra. Esta limitación metodológica ha sido reconocida en estudios de cohorte prospectivos de gran escala, en los cuales se ha observado que su incremento sostenido se asocia de manera consistente con mayor incidencia de enfermedad de cálculos biliares, particularmente en mujeres, lo que sugiere un efecto biológico más allá de su valor como simple indicador antropométrico global.
Diversos estudios prospectivos han demostrado que el incremento progresivo del índice de masa corporal se asocia con un aumento significativo del riesgo de formación de cálculos biliares de tipo colesterol. En cohortes amplias de mujeres seguidas durante varios años se ha observado una relación dosis respuesta, en la cual aumentos acumulados del índice de masa corporal se correlacionan con mayor incidencia de litiasis biliar sintomática. En particular, se ha descrito que incrementos clínicamente relevantes del índice de masa corporal, del orden de varios puntos, se acompañan de elevaciones progresivas del riesgo relativo de enfermedad biliar, lo cual ha sido interpretado como evidencia de un efecto continuo de la adiposidad sobre la saturación biliar de colesterol.
La mayor fuerza de asociación observada en mujeres en comparación con hombres ha sido reproducida en múltiples análisis epidemiológicos, lo que ha llevado a considerar la existencia de factores hormonales moduladores del metabolismo del colesterol biliar. Entre estos factores, los estrógenos desempeñan un papel central, ya que incrementan la síntesis hepática de colesterol mediante la regulación de la actividad de enzimas clave en la esteroidogénesis hepática, lo que conduce a una mayor secreción de colesterol hacia la bilis y a un aumento del índice de saturación de colesterol biliar. Este fenómeno favorece la nucleación de cristales de monohidrato de colesterol, etapa inicial en la formación de cálculos biliares.
La evidencia experimental y clínica ha mostrado que la exposición a estrógenos se asocia con un aumento en la secreción biliar de colesterol independiente del consumo dietético, lo que refuerza la hipótesis de que el sexo femenino presenta una predisposición biológica intrínseca a la litogénesis biliar. Esta diferencia contribuye a explicar por qué, aun a igualdad de índice de masa corporal, la incidencia de cálculos biliares es mayor en mujeres que en hombres en múltiples poblaciones estudiadas.
En relación con los mecanismos fisiopatológicos que vinculan la obesidad con la litiasis biliar, se ha descrito que la hiperinsulinemia crónica desempeña un papel relevante. La insulina, en concentraciones elevadas, incrementa la actividad de la enzima 3-hidroxi-3-metilglutaril coenzima A reductasa en el hepatocito, enzima limitante en la síntesis de colesterol endógeno. Este aumento en la actividad enzimática conduce a una mayor producción hepática de colesterol, que posteriormente es secretado a la bilis, incrementando su sobresaturación y favoreciendo la cristalización.
Este mecanismo se integra dentro de un contexto metabólico más amplio en el cual la resistencia a la insulina, frecuente en la obesidad visceral, potencia la síntesis hepática de lipoproteínas y altera el metabolismo de los ácidos biliares. Estudios fisiopatológicos han demostrado que la hiperinsulinemia no solamente incrementa la producción de colesterol, sino que también modifica la motilidad vesicular, lo que prolonga el tiempo de residencia de la bilis en la vesícula biliar y facilita la agregación de cristales.
Diversos estudios analíticos han evaluado qué medidas antropométricas presentan mayor capacidad predictiva para estimar el riesgo de desarrollar cálculos biliares. Entre estas medidas, la circunferencia abdominal y la relación cintura cadera han mostrado una asociación más fuerte con la presencia de adiposidad visceral, la cual es metabólicamente más activa que la adiposidad subcutánea y se relaciona de manera directa con alteraciones en el metabolismo lipídico y glucídico.
La evidencia epidemiológica indica que tanto el índice de masa corporal como la circunferencia abdominal se asocian de forma independiente con el riesgo de litiasis biliar en hombres y mujeres, aunque la combinación de múltiples indicadores antropométricos mejora la capacidad predictiva del riesgo. En mujeres, la combinación del índice de masa corporal con la relación cintura cadera ha mostrado un incremento en la precisión para identificar individuos con mayor probabilidad de desarrollar cálculos biliares, lo que sugiere un efecto sinérgico entre adiposidad total y distribución central de grasa.
En hombres, se ha observado que concentraciones bajas de colesterol de lipoproteínas de alta densidad constituyen un factor de riesgo independiente para la formación de cálculos biliares, lo que refleja alteraciones en el transporte reverso de colesterol y en la homeostasis lipídica sistémica. En mujeres, tanto el índice de masa corporal elevado como la disminución del colesterol de lipoproteínas de alta densidad han sido identificados como factores independientes asociados a mayor riesgo de enfermedad litiásica biliar.
El incremento simultáneo del índice de masa corporal, la circunferencia de cintura y el perímetro abdominal se ha asociado consistentemente con mayor riesgo de formación de cálculos biliares en ambos sexos, lo que refuerza la hipótesis de que la adiposidad central desempeña un papel fundamental en la fisiopatología de la enfermedad. Este patrón sugiere que no solamente la cantidad total de grasa corporal es relevante, sino también su distribución anatómica y su actividad metabólica.
Aunque la obesidad y el sobrepeso han sido establecidos como factores de riesgo independientes para la enfermedad litiásica biliar, también se ha observado que individuos con índice de masa corporal dentro de rangos considerados normales pueden desarrollar cálculos biliares. Este fenómeno ha sido atribuido a la existencia de factores genéticos que alteran el metabolismo del colesterol biliar y la motilidad vesicular, lo que incrementa la susceptibilidad individual a la cristalización incluso en ausencia de obesidad manifiesta.
Entre los factores hormonales y metabólicos implicados en la patogénesis de los cálculos biliares se encuentra la leptina, hormona secretada principalmente por el tejido adiposo blanco. La leptina participa en la regulación del apetito y del gasto energético, pero también influye en la distribución de la grasa corporal y en la sensibilidad a la insulina. Se ha descrito que variantes del gen del receptor de leptina se asocian con patrones específicos de distribución adiposa, lo cual puede modificar indirectamente el riesgo de litogénesis biliar.
Algunos estudios experimentales sugieren que la resistencia a la acción de la leptina podría asociarse con modificaciones en la formación de cristales de colesterol en la bilis, posiblemente a través de su interacción con vías metabólicas hepáticas y con la regulación de la secreción de colesterol. Sin embargo, este mecanismo aún se considera en investigación activa y requiere mayor evidencia experimental para su consolidación fisiopatológica definitiva.

Fuente y lecturas recomendadas:
- Carey, M. C., Paigen, B., & Nguyen, T. (1996). Pathogenesis of gallstones. Annual Review of Physiology, 58, 645–667.
- Portincasa, P., Moschetta, A., & Palasciano, G. (2006). Cholesterol gallstone disease. The Lancet, 368(9531), 230–239.
- Stinton, L. M., & Shaffer, E. A. (2012). Epidemiology of gallbladder disease: Cholelithiasis and cancer. Gut and Liver, 6(2), 172–187.
- Wang, D. Q. H., Afdhal, N. H., & Carey, M. C. (2009). Gallstone disease. New England Journal of Medicine, 360(19), 1981–1990.
- Biddinger, S. B., Haas, J. T., Yu, B. B., Bezy, O., Jing, E., Zhang, W., Unterman, T. G., & Kahn, C. R. (2008). Hepatic insulin resistance directly promotes formation of cholesterol gallstones. Nature Medicine, 14(7), 778–782.
- Méndez-Sánchez, N., King-Martínez, A. C., & Uribe, M. (2007). The role of diet in cholesterol gallstone formation. Clinical Nutrition, 26(1), 1–10.
- Ko, C. W., & Lee, S. P. (2002). Gallstones and the risk of gallbladder cancer. Best Practice & Research Clinical Gastroenterology, 20(6), 1135–1146.
- Shaffer, E. A. (2006). Gallstone disease: Epidemiology of gallbladder stone disease. Best Practice & Research Clinical Gastroenterology, 20(6), 981–996.