La formación de osteoblastos a partir de células madre mesenquimales representa un ejemplo paradigmático de diferenciación celular dirigida, en el cual una célula con amplio potencial de destino reduce progresivamente sus posibilidades hasta adquirir un fenotipo altamente especializado. Este proceso no es arbitrario, sino que responde a una lógica biológica profundamente integrada en la organización del tejido óseo y en las necesidades fisiológicas del organismo.
Las células madre mesenquimales, localizadas principalmente en la médula ósea, constituyen una población celular con capacidad multipotente, lo que significa que pueden generar distintos tipos celulares del linaje mesodérmico. Esta versatilidad no implica una elección aleatoria de destino, sino que está determinada por señales específicas del microambiente en el que se encuentran. Dicho microambiente, también denominado nicho celular, está conformado por una compleja red de componentes extracelulares, gradientes de factores solubles, interacciones célula a célula y estímulos mecánicos. En función de esta integración de señales, las células madre mesenquimales activan programas génicos particulares que las conducen hacia la diferenciación en osteoblastos, adipocitos o condrocitos. Así, la multipotencialidad se traduce en una capacidad de respuesta adaptativa a las necesidades tisulares.
La decisión de adoptar un destino osteogénico se encuentra sometida a un control molecular extremadamente estricto. Entre los reguladores más influyentes destacan las proteínas morfogenéticas óseas y las vías de señalización WNT, las cuales actúan como verdaderos ejes organizadores de la diferenciación. Estas rutas no solo inducen la expresión de genes específicos del linaje osteoblástico, sino que también reprimen programas alternativos, como los asociados a la adipogénesis o la condrogénesis. Sin embargo, la regulación no se limita a estas vías principales; otros sistemas de señalización, como el del factor nuclear kappa B y la actividad de enzimas moduladoras de la cromatina como la sirtuina dependiente de nicotinamida adenina dinucleótido, participan en la modulación fina del proceso. Esto revela que la diferenciación osteogénica es el resultado de una red compleja de interacciones moleculares, más que de una única señal dominante.
Un aspecto particularmente interesante de este proceso es su carácter de retroalimentación positiva. La presencia de osteoblastos maduros en el entorno puede favorecer la diferenciación de nuevas células madre mesenquimales hacia el mismo linaje. Este fenómeno sugiere la existencia de mecanismos de amplificación local, mediante los cuales el tejido óseo en formación promueve su propia expansión. Parte de esta comunicación se realiza a través de factores solubles liberados al medio extracelular, pero también intervienen estructuras como las vesículas extracelulares, que transportan proteínas, lípidos y material genético capaces de modificar el comportamiento de células vecinas. Este sistema de señalización intercelular contribuye a coordinar la formación ósea en el espacio y en el tiempo.
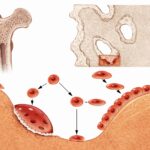
El proceso de diferenciación sigue una secuencia ordenada de etapas. Inicialmente, las células madre mesenquimales adquieren un compromiso hacia un progenitor osteocondral común, lo que refleja la estrecha relación evolutiva y funcional entre el tejido óseo y el cartilaginoso. Posteriormente, la activación de factores de transcripción específicos marca un punto de no retorno en la diferenciación. Entre estos factores destacan aquellos que actúan como reguladores maestros de la identidad osteoblástica, promoviendo la expresión de genes necesarios para la síntesis de la matriz ósea. A medida que la célula progresa hacia el estado de preosteoblasto, comienza a expresar proteínas características, como enzimas implicadas en la mineralización y componentes estructurales de la matriz extracelular. Estas moléculas no solo definen la identidad celular, sino que también participan activamente en la formación del tejido óseo.
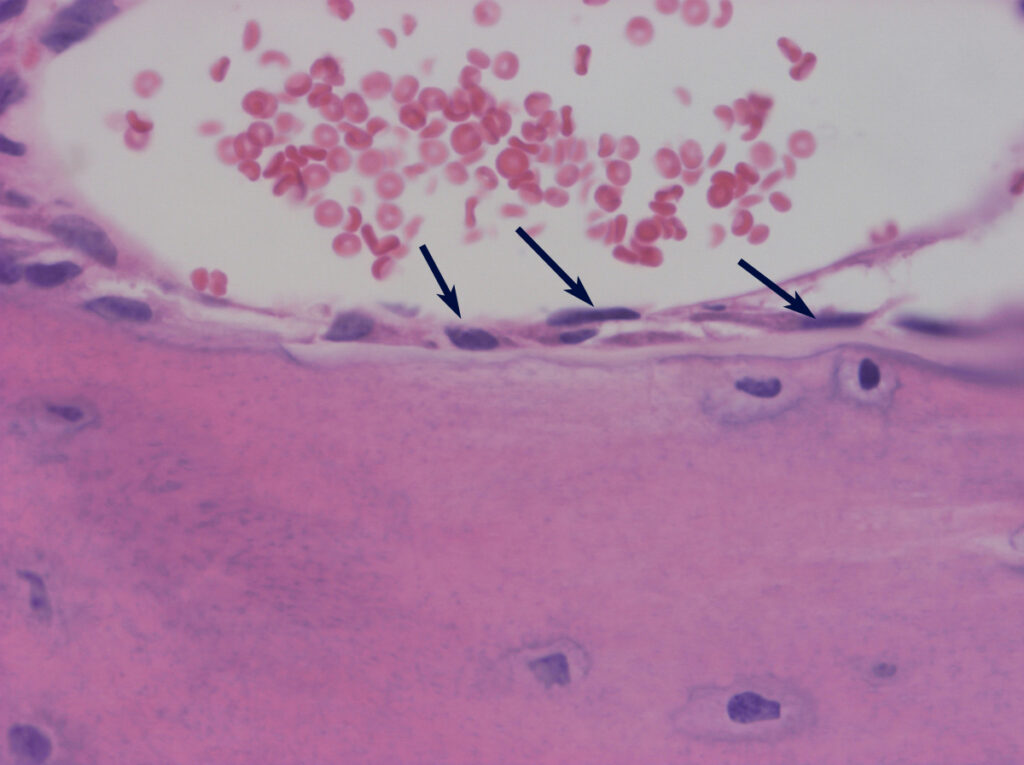
Una vez que los osteoblastos alcanzan su madurez y han cumplido su función de sintetizar y mineralizar la matriz ósea, no constituyen una población terminal homogénea, sino que pueden seguir distintos destinos según las necesidades del tejido. Una fracción de estas células experimenta muerte celular programada, lo cual permite eliminar células que ya no son necesarias y mantener el equilibrio tisular. Otra fracción se transforma en células de revestimiento óseo, que permanecen en la superficie del hueso formando una capa protectora. Estas células desempeñan un papel esencial en la regulación de la actividad de los osteoclastos, ya que controlan el acceso de estos a la superficie ósea y, por tanto, modulan el inicio de la resorción.
La función de las células de revestimiento puede entenderse como un mecanismo de “aislamiento funcional” del hueso. Al cubrir la superficie ósea, impiden que los osteoclastos entren en contacto directo con la matriz mineralizada, lo cual es un requisito indispensable para que estos completen su diferenciación y ejerzan su actividad resorbente. Sin embargo, esta barrera no es estática, sino dinámica: puede retirarse cuando el organismo requiere movilizar minerales o remodelar el tejido, y restablecerse posteriormente para proteger la integridad estructural.
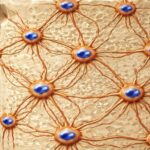
Otra vía de destino para los osteoblastos es su transformación en osteocitos, lo que implica un cambio profundo tanto en su morfología como en su función. Los osteocitos quedan atrapados dentro de la matriz ósea que ellos mismos han producido, adoptando una forma estrellada y estableciendo una extensa red de comunicación a través de prolongaciones citoplasmáticas. Esta disposición les permite actuar como sensores mecánicos altamente especializados. Detectan cambios en las fuerzas que actúan sobre el hueso y traducen esta información en señales bioquímicas que regulan la actividad de osteoblastos y osteoclastos. De este modo, los osteocitos desempeñan un papel central en la adaptación del tejido óseo a las cargas mecánicas.
Además de su función mecanosensora, los osteocitos participan en la regulación sistémica del metabolismo mineral, especialmente del fosfato. Mediante la secreción de factores específicos, influyen en órganos distantes, como el riñón, contribuyendo a mantener la homeostasis mineral del organismo. Este hecho pone de manifiesto que el tejido óseo no es únicamente una estructura de soporte, sino también un órgano con funciones endocrinas.
Finalmente, la apoptosis de los osteoblastos puede considerarse una estrategia de ajuste fino dentro del equilibrio tisular. Cuando no se requiere ni la formación de nuevas células de revestimiento ni la generación de osteocitos, la eliminación controlada de osteoblastos evita una acumulación innecesaria de células y contribuye a mantener la organización del tejido.

Fuente y lecturas recomendadas:
- Ponzetti, M., & Rucci, N. (2021). Osteoblast Differentiation and Signaling: Established Concepts and Emerging Topics. International journal of molecular sciences, 22(13), 6651. https://doi.org/10.3390/ijms22136651