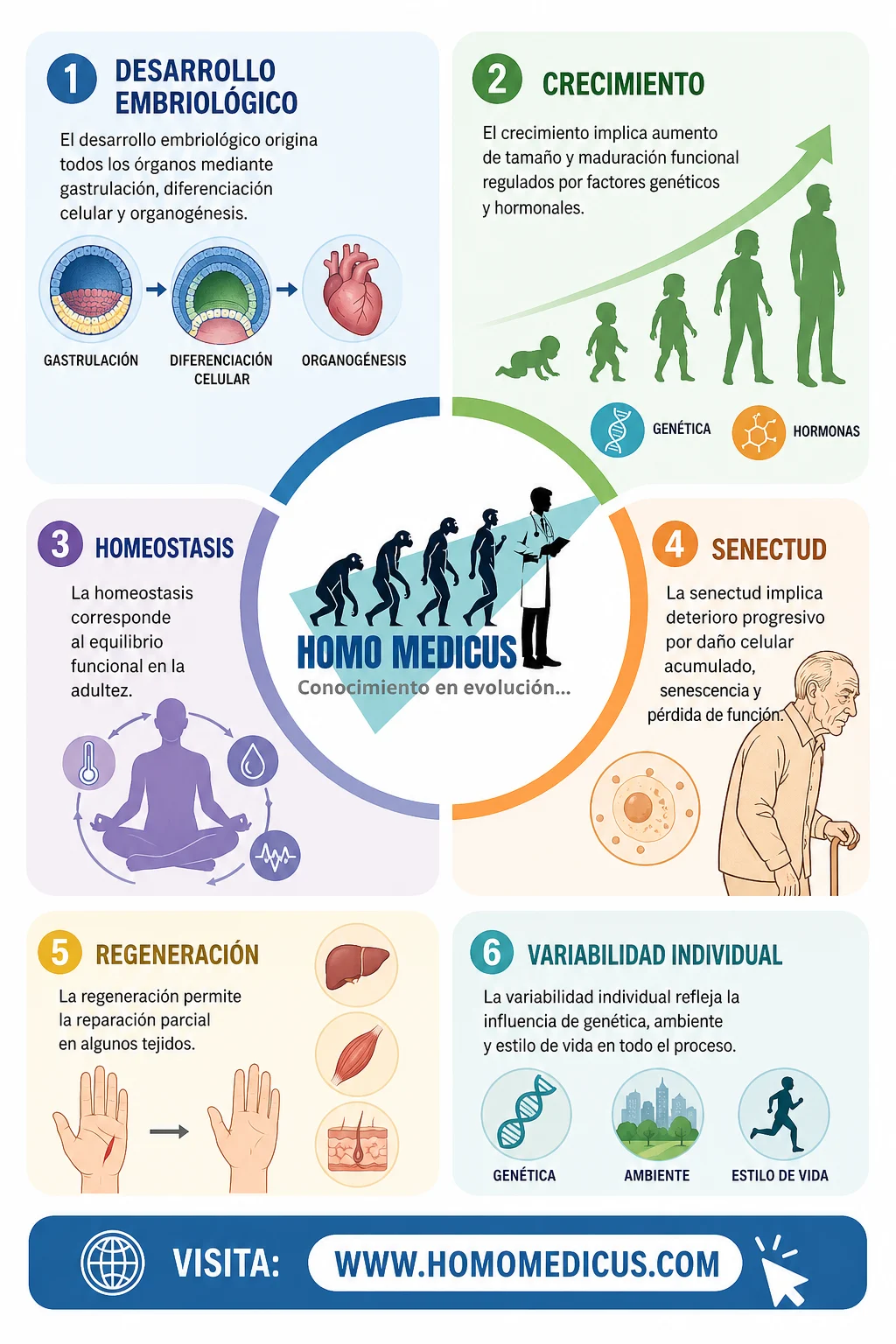
El desarrollo, crecimiento y envejecimiento de los órganos humanos constituyen un continuo biológico altamente regulado que integra procesos moleculares, celulares, tisulares y sistémicos. Desde la fecundación hasta la senectud, cada órgano atraviesa transformaciones dinámicas que reflejan tanto la programación genética como la interacción constante con el entorno. Este proceso no es lineal ni uniforme, sino que implica fases de proliferación, diferenciación, maduración funcional y, finalmente, declive progresivo asociado al envejecimiento.
Durante el desarrollo embriológico, el organismo humano se origina a partir de una sola célula totipotente, el cigoto, que experimenta divisiones mitóticas sucesivas generando blastómeros que progresivamente pierden totipotencia y adquieren destinos celulares específicos. La formación de las tres capas germinales —ectodermo, mesodermo y endodermo— constituye un evento crítico denominado gastrulación, el cual establece el plano corporal y determina el origen de todos los tejidos y órganos. A partir de estas capas, la organogénesis implica procesos altamente coordinados de señalización molecular, incluyendo gradientes de morfógenos, expresión génica diferencial y migración celular dirigida, que permiten la formación tridimensional de estructuras complejas.
El sistema nervioso, por ejemplo, deriva del ectodermo mediante la formación del tubo neural, cuyo cierre adecuado es esencial para evitar defectos congénitos. La evidencia experimental demuestra que la regulación de factores como Sonic Hedgehog y Bone Morphogenetic Proteins dirige la polaridad dorsoventral del tubo neural, estableciendo regiones funcionales específicas. La alteración de estas rutas puede generar malformaciones severas, lo que evidencia la precisión del control embriológico.
En el caso del sistema cardiovascular, el corazón es uno de los primeros órganos en formarse y funcionar, iniciando contracciones alrededor de la tercera semana de desarrollo. Este órgano surge del mesodermo esplácnico y experimenta un proceso de plegamiento y tabicación que da lugar a sus cuatro cavidades definitivas. Estudios embriológicos han demostrado que factores de transcripción como NKX2-5 y GATA4 son esenciales para la correcta morfogénesis cardíaca, regulando la diferenciación de cardiomiocitos y la formación del sistema de conducción.
Una vez concluida la organogénesis, los órganos entran en fases de crecimiento y maduración. Este crecimiento está mediado por una combinación de hiperplasia, aumento del número de células, e hipertrofia, incremento del tamaño celular. Durante la infancia y adolescencia, hormonas como la hormona del crecimiento, el factor de crecimiento similar a la insulina tipo 1 y las hormonas sexuales desempeñan un papel central en la expansión tisular y la adquisición de funciones especializadas.
El sistema esquelético ejemplifica este proceso de manera clara. Los huesos largos crecen mediante osificación endocondral en las placas epifisarias, donde condrocitos proliferan, se hipertrofian y son reemplazados por tejido óseo. Este mecanismo continúa hasta el cierre epifisario durante la adultez temprana, regulado principalmente por estrógenos. La persistencia o alteración de estas señales puede modificar la talla final o generar patologías como gigantismo o enanismo.
Los pulmones, por su parte, experimentan una maduración progresiva que culmina después del nacimiento. La formación de alvéolos funcionales continúa durante los primeros años de vida, lo que permite un incremento significativo en la capacidad de intercambio gaseoso. Este desarrollo posnatal explica la vulnerabilidad de los neonatos prematuros, cuyos pulmones no han completado la producción de surfactante, sustancia crucial para evitar el colapso alveolar.
A medida que el organismo alcanza la adultez, los órganos logran un equilibrio homeostático caracterizado por la estabilidad funcional. Sin embargo, este equilibrio es transitorio y progresivamente se ve afectado por procesos de envejecimiento. La senectud implica cambios acumulativos a nivel molecular, como daño al ácido desoxirribonucleico, acortamiento de telómeros, alteraciones epigenéticas y disfunción mitocondrial. Estos eventos conducen a una disminución en la capacidad regenerativa y funcional de los tejidos.
En el sistema cardiovascular, el envejecimiento se asocia con rigidez arterial debido a la acumulación de colágeno y la fragmentación de elastina. Esto incrementa la resistencia vascular y contribuye al desarrollo de hipertensión. Además, los cardiomiocitos muestran una menor capacidad contráctil y una respuesta reducida a estímulos β-adrenérgicos, lo que limita la adaptación del corazón al estrés fisiológico.
En el riñón, se observa una reducción progresiva del número de nefronas funcionales, acompañada de esclerosis glomerular y disminución del flujo sanguíneo renal. Esto se traduce en una reducción de la tasa de filtración glomerular, lo que afecta la capacidad de eliminar desechos metabólicos y mantener el equilibrio hidroelectrolítico.
El tejido óseo también experimenta cambios significativos, caracterizados por un desequilibrio entre la resorción osteoclástica y la formación osteoblástica. Este fenómeno conduce a una disminución de la densidad mineral ósea, aumentando el riesgo de fracturas. La osteoporosis es una manifestación clínica común de este proceso, particularmente en mujeres posmenopáusicas debido a la disminución de estrógenos.
A pesar de estos cambios degenerativos, ciertos órganos conservan una notable capacidad de regeneración. El hígado, por ejemplo, puede restaurar su masa funcional tras lesiones significativas mediante proliferación de hepatocitos. Este proceso está mediado por factores de crecimiento como hepatocyte growth factor y transforming growth factor alpha. La piel también mantiene una capacidad regenerativa continua gracias a la presencia de células madre en la capa basal de la epidermis.
La variabilidad individual en estos procesos refleja la interacción entre factores genéticos, ambientales y conductuales. La nutrición, el ejercicio, la exposición a toxinas y el estado de salud general modulan significativamente la velocidad y magnitud del envejecimiento orgánico. Estudios epidemiológicos han demostrado que estilos de vida saludables pueden retrasar la aparición de enfermedades relacionadas con la edad y preservar la función orgánica durante más tiempo.

Fuente y lecturas recomendadas:
- Sadler, T. W. (2019). Langman. Embriología médica. Wolters Kluwer.
- Gilbert, S. F. (2016). Developmental Biology. Sinauer Associates.
- Hall, J. E. (2021). Guyton and Hall Textbook of Medical Physiology. Elsevier.
- López-Otín, C., Blasco, M. A., Partridge, L., Serrano, M., Kroemer, G. (2013). The hallmarks of aging. Cell, 153(6), 1194–1217.
- Seeman, T. E., Merkin, S. S., Crimmins, E. M., Karlamangla, A. S. (2010). Disability trends among older Americans. Proceedings of the National Academy of Sciences, 107(47), 20234–20239.
- Kumar, V., Abbas, A. K., Aster, J. C. (2020). Robbins and Cotran Pathologic Basis of Disease. Elsevier.
- Campisi, J., d’Adda di Fagagna, F. (2007). Cellular senescence. Nature Reviews Molecular Cell Biology, 8(9), 729–740.




